Elettrolisi dell'Acqua: La Chiave per un Futuro Energetico Sostenibile
L'elettrolisi dell'acqua rappresenta una frontiera promettente per la produzione di idrogeno, un vettore energetico con il potenziale di rivoluzionare il nostro approccio all'energia. Questo processo, che utilizza l'elettricità per scindere l'acqua in idrogeno e ossigeno, si svolge all'interno di un dispositivo chiamato elettrolizzatore. L'integrazione della produzione di idrogeno tramite elettrolisi con fonti di energia rinnovabile, in particolare l'energia eolica, offre notevoli opportunità di sinergia. Nonostante la continua diminuzione dei costi dell'energia eolica, la sua intrinseca variabilità rappresenta una sfida per un utilizzo efficace. L'integrazione di combustibile idrogeno e generazione di energia elettrica in un parco eolico può fornire la flessibilità necessaria per allineare la produzione energetica alla disponibilità delle risorse, alle esigenze operative del sistema e ai fattori di mercato.
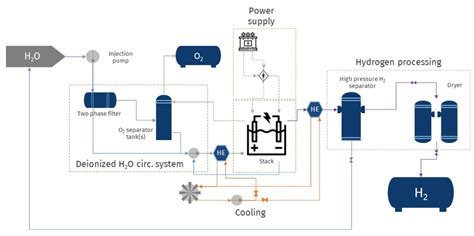
Il Processo Elettrolitico: Scomposizione dell'Acqua
L'elettrolisi scompone una materia prima, in questo caso l'acqua, nei suoi componenti elementari, idrogeno e ossigeno, attraverso l'impiego di elettricità. Gli elettrolizzatori sono costituiti da celle individuali e da un'unità di sistema centrale (bilanciamento dell'impianto). Tra le varie tecnologie di elettrolisi, l'elettrolisi degli ossidi solidi (SOE) è ancora in una fase avanzata di ricerca e sviluppo e i prodotti non sono ancora disponibili commercialmente.
L'efficienza di un processo elettrolitico è misurata dalla quantità di elettricità necessaria per produrre una determinata quantità di idrogeno. Sebbene gli elettrolizzatori siano già operativi, la ricerca continua a focalizzarsi sul loro miglioramento.
Elettrolisi ad Alta Temperatura: Maggiore Efficienza Energetica
L'elettrolisi ad alta temperatura (HTE) si dimostra economicamente più vantaggiosa rispetto all'elettrolisi tradizionale a temperatura ambiente. Questo perché una parte dell'energia è fornita sotto forma di calore, che è meno costoso dell'elettricità, e perché la reazione elettrolitica è più efficiente a temperature elevate. Infatti, a circa 2500 °C, l'energia elettrica non è più necessaria, poiché l'acqua si scinde in idrogeno e ossigeno tramite termolisi.
Il miglioramento dell'efficienza in questo tipo di elettrolisi è particolarmente apprezzabile quando l'elettricità utilizzata proviene da una macchina termica. In questo scenario, è fondamentale considerare la quantità di calore necessaria per produrre un chilogrammo di idrogeno (141,86 megajoule), sia nel processo HTE stesso che nella produzione dell'elettricità impiegata.
La scelta dei materiali per gli elettrodi e per l'elettrolita riveste un'importanza cruciale per l'efficienza e la durabilità del processo. Tuttavia, l'elettrolisi ad alta temperatura non elimina le inefficienze intrinseche delle macchine termiche, specialmente quando l'idrogeno prodotto viene successivamente riconvertito in elettricità in una cella a combustibile.
L'HTE, in sé, non può competere con la conversione chimica dell'energia proveniente dagli idrocarburi o dal carbone per la produzione di idrogeno, poiché queste ultime non sono limitate dall'efficienza delle macchine termiche.
Alternative alla Produzione di Idrogeno da Fonti Termiche
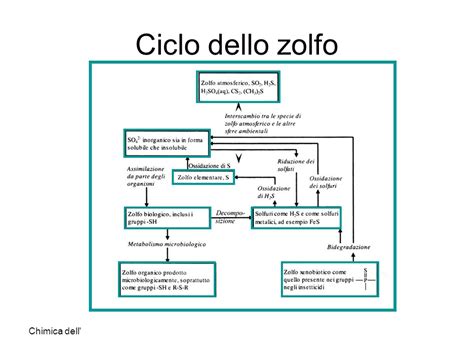
Nel caso di una fonte di calore economica ad alta temperatura, esistono altri metodi per la produzione di idrogeno. Tra questi, spicca il ciclo termochimico zolfo-iodio. La produzione termochimica ha il potenziale per raggiungere efficienze superiori all'HTE, poiché non richiede l'intermediazione di una macchina termica.
Il Mercato dell'Idrogeno: Un Settore in Crescita
Il mercato dell'idrogeno è considerevolmente vasto e in costante espansione. Nel 2004, il suo valore era di circa 135 miliardi di dollari all'anno, con una crescita annua stimata intorno al 10%. I principali consumatori di idrogeno sono attualmente le raffinerie di petrolio e le fabbriche di fertilizzanti, ognuna delle quali assorbe quasi la metà della produzione totale.
Efficienza Termodinamica e Bilancio Energetico
Durante il processo di elettrolisi, l'energia elettrica aggiunta è pari alla variazione dell'energia libera di Gibbs della reazione, più le perdite nel sistema. Teoricamente, le perdite possono essere ridotte a valori prossimi allo zero, il che implica che l'efficienza termodinamica massima di qualsiasi processo elettrochimico è del 100%.
Nella maggior parte dei casi, come nell'elettrolisi a temperatura ambiente, l'energia elettrica fornita supera la variazione di entalpia della reazione, con parte dell'energia rilasciata sotto forma di calore. Tuttavia, in altri scenari, come nell'elettrolisi del vapore ad alta temperatura in idrogeno e ossigeno, si osserva il fenomeno opposto: il calore viene assorbito dall'ambiente e il potere calorifico dell'idrogeno prodotto supera l'energia elettrica fornita. In queste circostanze, l'efficienza relativa all'elettricità fornita può essere considerata superiore al 100%. L'efficienza massima teorica di una cella a combustibile è l'inverso di quella dell'elettrolisi.
Idrogeno: cos'è e perché è il combustibile ideale per la transizione energetica del futuro
L'Idrogeno nella Transizione Ecologica e nel Settore Agricolo
Nel contesto della transizione ecologica, l'idrogeno emerge come un'opzione energetica promettente, potenzialmente altamente sostenibile, anche per il settore agricolo. Nell'ambito automobilistico, l'Unione Europea sta promuovendo attivamente la sostituzione dei combustibili fossili con fonti energetiche rinnovabili. L'elettrificazione sta progredendo rapidamente, sebbene persistano criticità legate alla densità energetica delle batterie, essenziale per garantire un'autonomia operativa adeguata dei veicoli, e a un'infrastruttura di ricarica ancora insufficiente.
Tra le tecnologie attualmente praticabili, lo sfruttamento dell'idrogeno apre prospettive interessanti, anche per le diverse modalità di produzione. Con opportune modifiche, l'idrogeno può alimentare veicoli dotati di motori a combustione interna originariamente progettati per benzina o diesel. Un'alternativa valida è l'impiego di motori elettrici alimentati da celle a combustibile che utilizzano idrogeno per generare elettricità.
Il principale vantaggio dell'idrogeno come vettore energetico risiede nelle sue emissioni: quando impiegato in una cella a combustibile o in un motore a combustione interna, produce principalmente vapore acqueo, senza rilascio di CO2 in atmosfera. Tuttavia, è importante notare che la combustione di idrogeno nei motori a combustione interna presenta un rendimento modesto. Inoltre, le emissioni non si limitano al vapore acqueo, ma includono anche una quota di ossidi di azoto (NOx), derivanti dalla dispersione di vapori di olio lubrificante non intercettati dal sistema di recupero.
Il bilancio energetico complessivo, considerando i numerosi passaggi necessari per produrre e utilizzare l'idrogeno, risulta in un'efficienza globale piuttosto bassa. L'elettrolisi dell'acqua, una delle opzioni "verdi" più considerate, ha un rendimento del 60%. L'utilizzo successivo nelle celle a combustibile presenta un valore analogo. La combinazione di queste due trasformazioni riduce l'efficienza al 36%. Aggiungendo il rendimento del motore elettrico (circa 90%) per generare energia meccanica, il risultato finale si attesta intorno al 32%. Ciò significa che circa due terzi dell'energia elettrica inizialmente prodotta non sono disponibili per usi utili.
L'Idrogeno nel Settore dei Trattori
Diversi produttori leader nel mercato dei trattori hanno già presentato modelli, per lo più prototipali, alimentati a idrogeno. Questi includono trattori con motore elettrico alimentato da celle a combustibile e trattori con motore a combustione interna modificato.
Un esempio notevole è l'Helios di Fendt, parte del progetto H2AgrarProject, che ha realizzato due prototipi sperimentali. Questa macchina è dotata di cinque serbatoi di idrogeno sul tetto, per una capacità totale di 21 kg di gas, immagazzinato a circa 700 bar. L'idrogeno alimenta una cella a combustibile da 100 kW, che genera l'energia elettrica per azionare un motore con una potenza massima di 100 kW.

Al contrario, l'H2-Dual Power di New Holland è basato su un T5.140 AutoCommand, equipaggiato con un motore FPT Nef Stage 5 da 4500 cm³ di cilindrata. Questo propulsore è progettato per funzionare anche a idrogeno in miscela fino al 65% con il gasolio convenzionale. Sebbene questa soluzione non elimini l'uso di idrocarburi liquidi, permette di ridurre le emissioni di CO2 tra il 45% e il 65%, con una lieve diminuzione anche delle emissioni di NOx. Questa metodologia riprende la soluzione già adottata nel settore automotive con l'alimentazione mista gasolio-metano, sia per veicoli commerciali che per automobili.
Innovazione Avanzata nei Veicoli Autonomi a Idrogeno
Oltre ai numerosi progetti ancora in fase sperimentale, si segnala il prototipo cinese ET504-H, un veicolo a trazione elettrica con celle a combustibile alimentate a idrogeno, presentato a Luoyang, Cina, quattro anni fa. Questo trattore robot autonomo, privo di postazione di guida, può operare sia in modalità autonoma che tramite controllo remoto. È equipaggiato con un motore centrale per la trazione e motori ausiliari per il sollevatore e lo sterzo.
In Europa, Exxact Robotics ha recentemente presentato il Traxx Concept H2, un trattore robot scavallante da vigneto, anch'esso alimentato a idrogeno. Questo veicolo è dotato di una cella a combustibile abbinata a un piccolo pacco batterie, per una potenza complessiva di 35 kW. L'idrogeno è immagazzinato in due serbatoi pressurizzati con una capacità totale di 9 kg, che, secondo il costruttore, consentirebbe al robot di operare per un'intera giornata senza necessità di rifornimento.
Classificazione dell'Idrogeno: Un Arcobaleno di Colori Energetici
In relazione alla fonte energetica di partenza e ai processi adottati per la sua produzione, è prassi comune classificare l'idrogeno con determinati "colori", sebbene queste assegnazioni possano variare:
Idrogeno Grigio: Viene estratto da combustibili fossili, principalmente metano, tramite "steam reforming". Questo processo genera significative quantità di CO2, che vengono generalmente rilasciate in atmosfera. Attualmente, si stima che dal 95% al 99% dell'idrogeno sia prodotto in questo modo. A livello globale, negli ultimi anni, circa il 6% del gas naturale e il 2% del carbone sono stati destinati alla produzione di idrogeno, con conseguenti emissioni di CO2 pari a circa 830 milioni di tonnellate all'anno.
Idrogeno Blu: Viene prodotto con le stesse modalità dell'idrogeno grigio, ma la CO2 risultante viene catturata e immagazzinata. Questo processo comporta un dispendio energetico nettamente superiore, riducendo notevolmente l'efficienza complessiva.
Idrogeno Verde: Si ottiene dall'acqua tramite elettrolisi, utilizzando esclusivamente elettricità proveniente da fonti rinnovabili (come l'energia solare o eolica). La reazione avviene in celle elettrolitiche, dove due elettrodi (anodo e catodo) scindono la molecola dell'acqua, liberando idrogeno e ossigeno. Il rendimento di questo processo è di circa il 60%. Questo valore è decisamente inferiore rispetto a quello ottenibile immagazzinando la stessa energia elettrica in batterie al litio o al piombo, che raggiungono rendimenti superiori al 90%.
Per il comparto agricolo, un'ulteriore opzione interessante è l'idrogeno ottenuto dalla gassificazione delle biomasse. Le biomasse contengono tipicamente circa il 50% di carbonio, il 6% di idrogeno e il 41% di ossigeno. Tuttavia, si tratta di un processo complesso con un bilancio energetico di produzione piuttosto basso.
Alternative di Sfruttamento dell'Idrogeno
Cella a Combustibile
Analogamente a una "pila" ben nota, la cella a combustibile è costituita da un polo positivo e uno negativo. Permette di "isolare" l'elettrone contenuto in un atomo di idrogeno, generando così lo ione positivo H+. Questo ione si combina con l'ossigeno, producendo acqua.
Motore Endotermico Modificato
L'architettura di questo propulsore è tradizionale, comprendendo cilindri, pistoni, valvole e iniettori. Sebbene si tratti di una semplificazione rispetto alla base di partenza, è importante considerare che i motori endotermici, per loro natura, sono meno efficienti dei motori elettrici.
Stoccaggio dell'Idrogeno: Sicurezza e Materiali
Una delle questioni più delicate riguarda le bombole di stoccaggio dell'idrogeno, poiché il gas è compresso a centinaia di bar di pressione. La norma UNR134 specifica che i materiali idonei per la costruzione dei serbatoi di stoccaggio includono il GFRP (Glass Fiber Reinforced Polymer, polimero rinforzato con fibra di vetro) per il rivestimento esterno e il CFRP (Carbon Fiber Reinforced Polymers, polimeri rinforzati con fibra di carbonio) per quello interno.
Toyota Sperimenta con Motori a Combustione Interna a Idrogeno
Toyota, pur continuando a investire nella mobilità elettrica, sta esplorando una variante innovativa dell'utilizzo dell'idrogeno. L'azienda intende impiegare l'idrogeno come sostituto dei combustibili fossili convenzionali, iniettandolo direttamente nei cilindri di un motore molto simile a quelli alimentati a benzina. Il nuovo motore a idrogeno verrà testato nel motorsport, precisamente in una gara endurance asiatica, la Super Taikyu, montato su una Corolla Sport del team Orc Rookie Racing. Si tratta di un motore a tre cilindri turbo da 1,6 litri.
L'Elettrolisi in Laboratorio: Un Esperimento Didattico
L'acqua è un composto formato da due atomi di idrogeno (H) legati a un atomo di ossigeno (O). La produzione di idrogeno e ossigeno è possibile tramite diversi metodi; il più semplice da realizzare è un processo noto come idrolisi, o elettrolisi dell'acqua a temperatura ambiente.
L'apparecchio comunemente utilizzato in laboratorio per la verifica volumetrica delle quantità di gas prodotte è il voltametro di Hoffmann, con elettrodi di platino. Versando acqua e una piccola percentuale di acido solforico, si osserva la scissione dell'acqua.
Per un confronto visivo delle quantità di gas generate senza manipolare acidi (l'acido solforico è presente nelle batterie delle auto), è sufficiente riempire un contenitore con acqua di rubinetto. In questo contenitore si immergono due elettrodi, preferibilmente di platino, ma si possono utilizzare anche due viti in acciaio inossidabile. Applicando una corrente continua a bassa tensione, gli ioni presenti nell'acqua consentono il passaggio della corrente elettrica, provocando la formazione di piccole bolle di idrogeno sull'elettrodo negativo e di ossigeno su quello positivo.
Se gli elettrodi sono di platino puro, il rapporto tra i gas prodotti è di 2 atomi di idrogeno (2H2) e 1 di ossigeno (O2), ovvero un volume doppio di idrogeno rispetto all'ossigeno. Se gli elettrodi sono impuri o di metalli diversi dal platino, parte dell'ossigeno viene consumata in processi ossidativi sull'elettrodo positivo, riducendo la quantità di ossigeno sviluppato.
I gas vengono raccolti in provette separate, precedentemente riempite d'acqua e posizionate capovolte, parzialmente immerse nell'acqua, sopra gli elettrodi. Avviando il passaggio di corrente, in assenza di additivi nell'acqua, la reazione è piuttosto lenta. Per accelerare il processo, si può aggiungere all'acqua un po' di bicarbonato di sodio, facilmente reperibile nei supermercati. Questo additivo non è corrosivo come l'acido e funziona egregiamente.
Pazientando, si noterà che la provetta dell'idrogeno si riempirà per prima, con l'idrogeno che si accumula nella parte superiore, sostituendo progressivamente l'acqua che finirà nel contenitore. A quel punto, la provetta dell'ossigeno sarà riempita solo a metà di gas, mentre l'altra metà sarà ancora occupata dall'acqua.
Si preleva la provetta dell'idrogeno, mantenendola capovolta (poiché l'idrogeno è più leggero dell'aria), e si inserisce al suo interno uno stoppino acceso. Il gas non esplode, ma brucia; se ci si trova al buio, si potrà osservare la fiamma all'interno della provetta.
Successivamente, si riempie nuovamente la provetta con acqua e la si riposiziona capovolta sull'elettrodo, facendo ripartire l'elettrolisi fino a ottenere un nuovo riempimento. A questo punto, anche la provetta dell'ossigeno sarà piena.
Una volta che entrambe le provette sono piene di gas, si preleva quella dell'ossigeno, tappandone l'apertura con un dito mentre è ancora sott'acqua. Tolta dall'acqua e capovolta, tenendo l'apertura verso l'alto, si può rimuovere il dito. L'ossigeno, essendo più pesante dell'aria, rimarrà nella provetta. Inserendo lentamente dall'alto un legnetto acceso, anche senza fiamma viva ma con una brace all'estremità, e indirizzandolo verso il fondo, si osserverà che l'ossigeno riaccenderà la brace mantenendola viva fino all'esaurimento del gas.
Infine, si può ripetere l'esperimento precedente con la seconda provetta di idrogeno. In questo modo, si sono verificate le caratteristiche dei due gas ottenuti con l'idrolisi: l'idrogeno è un combustibile e l'ossigeno è un comburente.
tags: #elettrolisi #con #motorino
